Voda zapravo nije jedna tekućina, već dvije
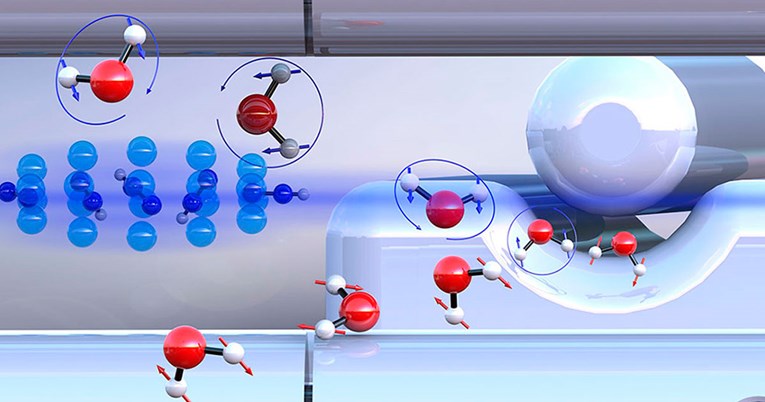
POSTOJE dva različita oblika molekula vode s gotovo identičnim fizikalnim svojstvima. Znanstvenici su napokon uspjeli odvojiti ta dva oblika te pokazati da oni mogu imati različitu kemijsku reaktivnost, prenosi Science Daily.
Do tih su otkrića došli istraživači sa Sveučilišta u Baselu i njihove kolege iz Hamburga. Objavili su ih u znanstvenom časopisu Nature Communications.
Iz kemijske perspektive, molekula vode sastoji se od jednog atoma kisika povezanog s dva atoma vodika. Manje je poznato da voda postoji u dva različita oblika (izomera) na molekularnoj razini.
Razlika leži u smjeru nuklearnih spinova dvaju atoma vodika. Ovisno o tome jesi li spinovi poravnani u istom ili suprotnom smjeru, postoji orto-voda i para-voda.
Eksperimenti sa sortiranim molekulama voda
Grupa istraživača na čelu s prof. Stefanom Willitschom s Odsjeka za kemiju Sveučilišta u Baselu istraživala je kako se ta dva oblika vode razlikuju po kemijskoj reaktivnosti, odnosno sposobnosti kemijskog reagiranja.
Oba izomera imaju gotovo identična fizikalna svojstva, zbog čega njihovo međusobno razdvajanje predstavlja veliki izazov. U novom istraživanju razdvajanje je omogućila metoda zasnovana na električnim poljima.
Pomoću tog pristupa, istraživači su uspjeli pokrenuti kontrolirane reakcije između presortiranih izomera vode i ultra hladnih iona diazenila ("protoniranog dušika" N2H+) u stupici. Tijekom tog postupka, diazenilov ion premješta svoj proton u molekulu vode.
Povećana reaktivnost
U studiji je dokazano da para-voda reagira oko 25 posto brže od orto-vode. To se može objasniti činjenicom da nuklearni spin također utječe na rotaciju molekula vode, stoga među reakcijskim partnerima postoje različite sile privlačenja.
Para-voda snažnije privlači svog reakcijskog partnera od orto-vode, što dovodi do povećane kemijske reaktivnosti. Računalne su simulacije potvrdile te rezultate.
Istraživači su u svojim eksperimentima radili s molekulama na veoma niskim temperaturama, blizu apsolutne nule (oko -273°C). To predstavlja idealne uvjete za preciznu pripremu pojedinih kvantnih stanja i određivanje energetskog sadržaja molekula te izazivanje kontrolirane reakcije među njima.
"Što bolje kontrolirate stanja molekula uključenih u kemijsku reakciju, bolje ćete moći istražiti i razumjeti temeljne mehanizme i dinamiku reakcije", objašnjava Willitsch.








































 Facebook
Facebook
 Google
Google